Химическая термодинамика: основные понятия, законы, задачи
Отдельные элементы основ химической термодинамики начинают рассматривать еще в средней школе. На уроках химии ученики впервые сталкиваются с такими понятиями, как обратимые и необратимые процессы, химическое равновесие, тепловой эффект и многими другими. Из школьного курса физики они узнают о внутренней энергии, работе, потенциалах и даже знакомятся с первым началом термодинамики.
Определение термодинамики
Студенты вузов и ссузов химико-технологических специальностей подробно изучают термодинамику в рамках физической и/или коллоидной химии. Это один из основополагающих предметов, понимание которого позволяет выполнять расчеты, необходимые для разработки новых технологических линий производства и оборудования для них, решения проблем в уже имеющихся технологических схемах.
Химической термодинамикой принято называть один из разделов физической химии, изучающий химические макросистемы и связанные с ними процессы на основе общих законов о превращениях теплоты, работы и энергии друг в друга.
Она основана на трех постулатах, которые чаще называют началами термодинамики. Они не имеют математической основы, а базируются на обобщении опытных данных, которые накоплены человечеством. Из этих законов выведены многочисленные следствия, положенные в основу описания окружающего мира.
Задачи
К основным задачам химической термодинамики можно отнести:
Предмет и объект
Данный раздел науки не ставит перед собой цели объяснить природу или механизм какого-либо химического явления. Ее интересует исключительно энергетическая сторона происходящих процессов. Поэтому предметом химической термодинамики можно назвать энергию и законы превращения энергии в ходе химических реакций, растворении веществ при испарении и кристаллизации.
Эта наука дает возможность судить о том, способна ли протекать та или иная реакция в определенных условиях именно с энергетической стороны вопроса.
Объектами ее изучения называют тепловые балансы физико-химических процессов, фазовые переходы и химические равновесия. Причем только в макроскопических системах, то есть таких, которые состоят из огромного числа частиц.
Методы
Термодинамический раздел физической химии для решения основных своих задач пользуется теоретическими (расчетными) и практическими (экспериментальными) методами. Первая группа методов позволяет количественно связать разные свойства, и рассчитать одни из них, основываясь на опытных величинах других, пользуясь принципами термодинамики. Законы квантовой механики помогают установить способы описания и особенности движения частиц, связать величины, характеризующие их, с физическими параметрами, определяемыми в ходе опытов.
Исследовательские методы химической термодинамики делят на две группы:
Оба этих подхода имеют свои достоинства и недостатки.
В связи с большой общностью достаточно прост и не требует дополнительных сведений, при этом решает конкретные задачи
Не раскрывает механизм процесса
Помогает понять суть и механизм явления, поскольку основан на представлениях об атомах и молекулах
Требует основательной подготовки и большого объема знаний
Основные понятия химической термодинамики
Система – это любой материальный макроскопический объект изучения, обособленный от внешней среды, причем граница может быть как реальной, так и воображаемой.
Для обозначения способа обмена энергией и веществом используют понятия тепловых, механических и диффузионных контактов.
Параметрами состояния системы называют любые измеряемые макрохарактеристики состояния системы. Они могут быть:
Все эти параметры заимствованы химической термодинамикой у физики и химии, но приобретают несколько иное содержание, поскольку рассматриваются в зависимости от температуры. Именно благодаря этой величине различные свойства связываются между собой.
Равновесным называют такое состоянием системы, в которое она приходит при постоянстве внешних условий и характеризуется временным постоянством термодинамических параметров, а также отсутствием в ней вещественных и тепловых потоков. Для данного состояния наблюдается постоянство давления, температуры и химического потенциала во всем объеме системы.
Равновесные и неравновесные процессы
В системе основных понятий химической термодинамики особое место занимает термодинамический процесс. Его определяют как изменения в состоянии системы, которые характеризуются изменениями одного или нескольких термодинамических параметров.
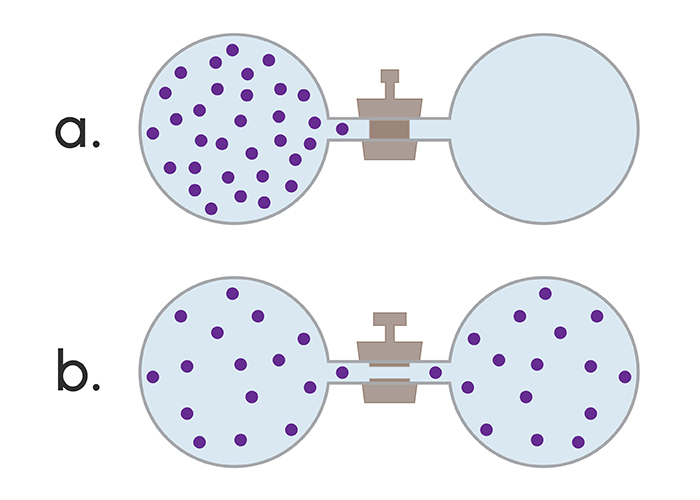
Изменения в состоянии системы возможны при разных условиях. В связи с этим различают равновесные и неравновесные процессы. Равновесный (или квазистатический) процесс рассматривается как ряд равновесных состояний какой-либо системы. При этом все параметры ее изменяются бесконечно медленно. Для протекания такого процесса необходимо соблюдение ряда условий:
Процесс изменения неравновесного состояния системы на равновесное называют релаксацией, а длительность его – временем релаксации. В химической термодинамике зачастую принимают наибольшее значение времени релаксации для какого-либо процесса. Связано это с тем, что реальные системы легко выходят из состояния равновесия возникающими потоками энергии и/или вещества в системе и являются неравновесными.
Обратимые и необратимые процессы
Обратимым термодинамическим процессом называют переход системы из одного ее состояния в другое. Он может протекать не только в прямом направлении, но и в обратном, причем через одни и те же промежуточные состояния, при этом изменений в окружающей среде наблюдаться не будет.
Необратимым называют процесс, для которого невозможен переход системы из одного ее состояние в другое, не сопровождающийся изменениями в окружающей среде.
Необратимыми процессами являются:
Другие виды термодинамических процессов
Круговым процессом (циклом) называют такой процесс, в ходе которого система характеризовалась изменением своих свойств, а в его конце вернулась к исходным значениям.
В зависимости от значений температуры, объема и давления, характеризующих процесс, в химической термодинамике различают следующие его виды:
Законы химической термодинамики
Прежде чем рассматривать основные постулаты, необходимо вспомнить суть величин, характеризующих состояние различных систем.
Под внутренней энергией U системы понимают запас ее энергии, складывающийся из энергий движения и взаимодействия частиц, то есть всех видов энергии за исключением кинетической энергии и ее потенциальной энергии положения. Определить ее изменение ∆U.
Энтальпию Н часто называют энергией расширенной системы, а также ее теплосодержанием. H=U+pV.
Теплотой Q называют неупорядоченную форму передачи энергии. Внутренняя теплота системы считается положительной (Q > 0), если тепло поглощается (эндотермический процесс). Отрицательна (Q 0), если совершается системой против внешних сил, и отрицательной (A 2 марта, 2018
Термодинамика строительства
Из чего возводят современное загородное жилье
Существует множество технологий, позволяющих построить красивый загородный дом или коттедж. Его можно сложить из кирпича или камня, срубить из дерева, собрать из пенобетонных блоков, шлаков и т.д. Все эти технологии появились в разное время и решали свои задачи: построить жилье быстро, построить жилье не из дерева в местности, где нет камня, построить жилье из недорогих материалов, сделать постройку жилья доступной для непрофессиональных строителей и т.д. Однако среди этих задач никогда не было такой актуальной, как энергосбережение. Естественно, не в ущерб таким качествам как надежность, долговечность, экологичность, экономичность и простота строительства.
Ответом на все вышеперечисленные требования современности стала технология «Термодом». Во второй половине прошлого столетия она отлично себя зарекомендовала в странах Европы и сегодня активно завоевывает позиции и в Украине. Все больше строителей отдает предпочтение именно этой технологии. «После 2004 года мы ежегодно отмечаем, кроме 2009 года, рост продаж на 30-50%», – говорит генеральный директор производственно-строительной компании «Валькирия» (производитель блоков несъемной опалубки из пенополистирола) Александр Бурлаченко.
Впрочем, говорить о повсеместном применении технологии «Термодом» пока рано. И тому есть несколько причин: приверженность потенциальных покупателей домов классическим традициям, нежелание переучиваться у строителей и «специализация» отечественной строительной промышленности под классические технологии.
Поэтому сегодня технологию «Термодом» выбирают те, кто не поленился глубоко изучить историю вопроса, сравнил самые перспективные технологии и сделал выбор в пользу комфорта, экологичности и энергосбережения.
40 лет назад
Родоначальником современной технологии «Термодом» стала технология PLASTBAU, которая появилась в Италии в 70-х годах прошлого века. В 1976 году компания Renova-Termodom наладила производство термоблоков в Германии, после чего технология начала распространятся по всему миру. Например, к началу 1999 года в Германии было построено более 25 тыс. домов из термоблоков. В знаменитой «Европейской деревне», построенной под Берлином по решению Европейского Сообщества, каждая из стран ЕС представляла свои наиболее передовые строительные технологии. Примечательно, что Германия представлена энергосберегающей технологией строительства «Термодом». В Польше принята специальная государственная программа «Теплый дом» и ежегодно строится более 5 тыс. домов из пенополистирола. Среди европейских стран, которые активно используют технологию «Термодом», стоит отметить Францию и скандинавские страны. Кроме Европы термодома строят в США, Канаде, Израиле, Панаме, ЮАР.
В Украине строительство домов из пенополистирольных блоков несъемной опалубки началось во второй половине 90-х, после того как в январе 1995 были приняты государственные строительные нормы, регламентирующие все вопросы строительства домов из пенополистирольных блоков несъемной опалубки (ДБН В.2.6-6-95).
Статьи по частному строительству
Быстрая приватизация земли, земельного участка под ключ, без Вашего участия, со 100% гарантиями.
До начала строительства «домика» для вашего автомобиля необходимо на его постройку получить разрешение. Для этого нужно обратиться в региональную проектную организацию, где заказать проект запланированного гаража. После готовности проекта, его нужно согласовать с коммунальными службами, а также с главным архитектором.
Пришло время поставить забор на вашем участке. Из какого материала сделать забор? Как правило, хочется недорого и в тоже время качественно. Существует только один такой материал – это профнастил. Установка забора из профнастила состоит из двух этапов: установка каркаса крепления профнастила и крепление самих листов профнастила.
Учебные пособия и методические указания / Химия в строительстве. Курс лекций. Григорьева Л.С
Григорьева Л.С. Химия в строительстве: Курс лекций. /Моск. гос. строит. ун-т. М.: МГСУ, 2010. – 104 с.
Конспект лекций по дисциплине «Химия в строительстве» составлен в соответствии с программой курса. В учебном пособии рассмотрены основы химической термодинамики, термохимии, поверхностных явлений. Даны классификации дисперсных систем. Представлены теоретические основы коррозионных процессов. Учебное пособие предназначено для студентов строительных вузов.
Р е ц е н з е н т ы
проф., канд. техн. наук А.М. Орлова, проф., д-р техн. наук, зав. лаб ИНЭОС РАН А.А. Аскадский
Компьютерная правка и верстка О.В. Суховой
Лицензия ЛР №020675 от 09.12.97 г.
Подписано в печать 25.01. 2010 г.
ГОУ ВПО Московский государственный строительный университет.
Ред.-изд. отдел. Тел. (499) 183-97-95, e-mail rio@mgsu.ru. Типография МГСУ. Тел. (499) 183-91-90, (499) 183-67-92, (499) 183-91-44
Л е к ц и я 1. ОСНОВЫ ТЕРМОДИНАМИКИ
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ЗАКОН ГЕССА
Современное строительство использует великое множество самых разнообразных строительных материалов, из которых при помощи определенных строительных технологий и строится здание или сооружение. Основой технологических процессов, как производства строительных материалов, так и собственно технологии строительного производства являются основные законы природы. Поэтому при возведении любого здания необходимо учитывать самые разнообразные химические и физические процессы, происходящие в материалах при строительстве, сразу же после него или в процессе эксплуатации.
Теоретическим фундаментом таких процессов, прежде всего, являются основные положения термодинамики и, в частности, химической термодинамики.
Основываясь на теоретических положениях химической термодинамики можно рассчитывать и прогнозировать прочность твердых тел, устойчивость гидратных образований, определяющих прочность бетонов, обосновывать направление, по которому протекают процессы гидратации минеральных вяжущих. Знание максимального тепловыделения, скорости этого процесса необходимо при выборе цемента для гидротехнических и иных видов строительства. Без термодинамического анализа трудно оценить процессы коррозии строительных материалов и их защиты.
Классическая термодинамика первоначально занималась изучением теплоты, но в дальнейшем, она включила изучение превращений энергии во всех её формах.
Химическая термодинамика изучает:
1. Соотношения между теплотой и другими формами энергии в процессе химических реакций;
2. Возможность самопроизвольного протекания химических реакций в данных условиях;
3. Условия, при которых реакция находится в состоянии химического равновесия.
Термодинамика оперирует понятиями система, термодинамический процесс. Система – совокупность тел, выделенных фактически
или мысленно из окружающей среды и находящихся во взаимодействии с окружающей средой. Если между этой системой и средой отсутствует какой-либо обмен энергией и веществом, то она называется изолированной (объем и энергия такой системы постоянны). Система называется закрытой, если между системой, и средой взаимодействие осуществляется только за счет обмена энергией, но без обмена веществом.
Система называется открытой, если взаимодействие между системой и средой выражается как в обмене энергией, так и в обмене веществом.
Термодинамический процесс – совокупность последовательных состояний, через которые проходит термодинамическая система при её взаимодействии с окружающей средой.
Состояние системы характеризуют параметрами: объемом V, давлением р, температурой Т, концентрацией С и т. д.
Параметры, не зависящие от пути перехода системы из одного состояния в другое, а зависящие только от начального и конечного состояний, называют функциями состояния, например, внутренняя энергия тела. Эта энергия складывается из кинетической энергии молекул, энергии колебательного движения атомов, энергии электронов, внутриядерной энергии, энергии взаимодействия молекул и т.д., за исключением кинетической энергии системы в целом и потенциальной энергии ее положения в пространстве.
Все изменения внутренней энергии при ее переходе от одного тела к другому можно разбить на две группы. В первую группу входит форма перехода энергии за счет хаотического столкновения молекул двух соприкасающихся тел. Мерой передаваемой таким способом энергии является теплота.
Теплота представлена интенсивным хаотическим движением молекул и атомов, из которых это вещество состоит, т.е неупорядоченным движением микрочастиц.
Во вторую группу входят многие формы перехода энергии при перемещении масс, состоящих из большого числа частиц, под дейст-
вием каких-либо сил. Общей мерой, передаваемой таким образом энергии является работа, т.е. работа включает в себя упорядоченную макроскопическую форму движения.
Теплота Q и работа А в общем виде не являются функциями состояния и характеризуют способы передачи энергии.
Взаимосвязь между внутренней энергией, теплотой и работой устанавливается на основе первого начала термодинамики.
Первое начало (закон) термодинамики непосредственно связано с законом сохранения и превращения энергии, который устанавливает эквивалентность ее форм. Этот закон является универсальным и подтверждается всем опытом человечества
«Во всех явлениях природы энергия не может исчезнуть бесследно или возникнуть из ничего. Энергия только превращается из одной формы в другую в строго эквивалентных соотношениях». Иногда этот закон формулируют в другой форме:
«Вечный двигатель первого рода невозможен, т.е. невозможно построить машину, которая выполняла бы механическую работу, не затрачивая на это соответствующего количества молекулярной энергии».
«В изолированной системе внутренняя энергия постоянна и определяется природой составляющих ее веществ, их массой и условиями существования».
Внутренняя энергия может изменяться только под влиянием внешних воздействий, то есть в результате сообщения системе количества теплоты Q и совершения над ней работы (А).
Условились считать положительными величинами теплоту, полученную системой, и работу, совершенную системой. Тогда из первого начала термодинамики следует, что теплота, подводимая к системе, идет на приращение внутренней энергии системы и на совер-
шение работы против внешних сил:
Данное уравнение представляет собой математическую форму-
лировку первого закона термодинамики.
При изохорном процессе (V = const)
теплота равна прираще-
нию внутренней энергии
т.е. все тепло расходуется на изменение внутренней энергии. Уравнение первого начала термодинамики применительно к изобарным процессам, в которых совершается только работа расши-