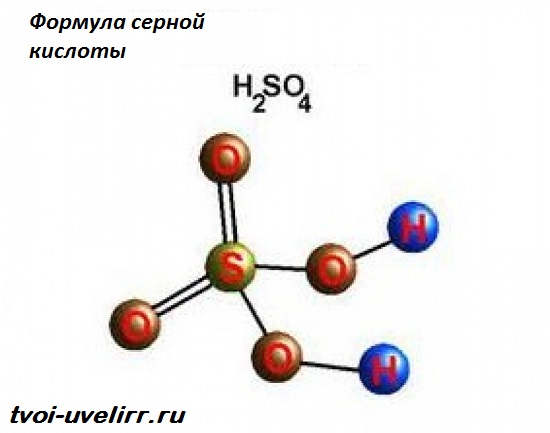
Серная кислота
Концентрированная серная кислота очень бурно реагирует с водой, так как при этом выделяется большое количество тепла (19 ккал на моль кислоты) вследствие образования гидратов. По этой причине следует всегда разбавлять серную кислоту, наливая её в воду, а не наоборот.
Серная кислота обладает высокой гигроскопичностью, то есть хорошо поглощает водные пары из воздуха, поэтому может применяться для осушения газов, не реагирующих с нею. Гигроскопичностью обьясняется и обугливание органических веществ, к примеру, сахара или дерева, при воздействии на них концентрированной серной кислотой. При этом образуются гидраты серной кислоты. Также из-за малой летучести её используют для вытеснения других, более летучих кислот из их солей.
Концентрированная серная кислота является сильным окислителем. Она окисляет металлы, стоящие в ряду напряжений до серебра включительно, а продукты реакции зависят от условий ее проведения и активности самого металла. Образует два ряда солей: средние — сульфаты и кислые — гидросульфаты, а также эфиры.
Разбавленная серная кислота взаимодействует со всеми металлами, находящимися в электрохимическом ряду напряжений левее водорода (H), с выделением Н2, окислительные свойства для нее нехарактерны.
В промышленности серная кислота получают двумя методами: контактный метод с использованием твердых катализаторов (контактов), и нитрозный — с оксидами азота. Сырьём служат сера, сульфиды металлов и т.п. Выпускается кислота нескольких сортов, в зависимости от чистоты и концентрации: аккумуляторная(самая чистая), техническая,башенная, купоросное масло, олеум(раствор серного ангидрида в серной кислоте).
Применение серной кислоты:
Применение серной кислоты в промышленности
Пищевая промышленность знакома с серной кислотой в виде пищевой добавки Е513. Кислота выступает в качестве эмульгатора. Данная пищевая добавка используется для изготовления напитков. С её помощью регулируется кислотность. Помимо пищи, Е513 входит в состав минеральных удобрений. Применение серной кислоты в промышленности имеет широкое распространение. Промышленный органический синтез использует серную кислоту для проведения следующих реакций: алкилирование, дегидратация, гидратация. С помощью данной кислоты восстанавливается необходимое количество смол на фильтрах, что используются на производстве дистилированной воды.
Применение серной кислоты в быту
Серная кислота в домашних условиях пользуется спросом среди автолюбителей. Процесс приготовления раствора электролита для автомобильного аккумулятора сопровождается добавление серной кислоты. Работая с данной кислотой следует помнить о правилах безопасности. В случае попадания кислоты на одежду или открытые участки кожи, стоит немедленно промыть их проточной водой. Серная кислота, которая разлилась на металл, может нейтрализоваться с помощью извести или мела. Заправляя автомобильный аккумулятор необходимо придерживаться некой последовательности: постепенно добавлять кислоту к воде, а не наоборот. Когда вода вступает в реакцию с серной кислотой происходит сильное нагревание жидкости, что может приводить к её разбрызгиванию. Поэтому стоит быть особо внимательным, чтобы жидкость не попала на лицо, или в глаза. Кислота должна храниться в плотно закрытой емкости. Важно, чтобы химическое вещество сохранялось в недоступном для детей месте.
Применение серной кислоты в медицине
В медицине нашлось широкое применение солей серной кислоты. К примеру, магний сульфат назначается людям с целью достичь слабительного эффекта. Еще одним производным серной кислоты есть натрий тиосульфат. Лекарственное средство используется в роли противоядия в случае отправления следующими веществами: ртуть, свинец, галогены, цианид. Тиосульфат натрий вместе с соляной кислотой используется для лечения дерматологических заболеваний. Профессор Демьянович предложил союз этих двух препаратов для лечения чесотки. В виде водного раствора, натрий тиосульфат вводят людям, которые страдают аллергическими недугами.
Магния сульфат обладает широким спектром возможностей. Поэтому применяется врачами различных специальностей. В качестве спазмолитика магний сульфат вводят больным при гипертонической болезни. Если у человека присутствуют заболевания желчного пузыря, вещество вводится внутрь для улучшение желчеотделения. Применение серной кислоты в медицине в виде магния сульфата в гинекологической практике встречается часто. Гинекологи помогают роженицам посредством введения магния сульфата внутримышечно, таким способом они обезболивают роды. Помимо всех выше указанных свойств, магний сульфат обладает антисудорожным эффектом.
Применение серной кислоты в производстве
Серная кислота, области применение которой разнообразны, используется так же при производстве минеральных удобрений. Для более удобного сотрудничества, заводы,что занимаются производством серной кислоты и минеральных удобрений, в основном, расположены поблизости друг от друга. Этот момент создает непрерывное производство.
Применение серной кислоты в изготовлении красителей и синтетических волокон занимает второе место по распространенности после производства минеральных удобрений. Многие отрасли промышленности используют серную кислоту в некоторых процессах на производстве. Применение серной кислоты нашло спрос и в быту. Люди пользуются химическим веществом для обслуживания своих автомобилей. Приобрести серную кислоту возможно в магазинах, что имеют специализацию по продаже химических веществ, в том числе у нас по ссылке. Серная кислота транспортируется соответственно правилам перевозки подобного груза. Железнодорожный или автомобильный транспорт перевозит кислоту в соответствующих емкостях. В первом случае в качестве емкости выступает цистерна, во втором – бочка или контейнер.
Особенности применения и биологическая опасность
Не нашли что искали? Вы можете оставить заявку, в форме обратной связи.
Серная кислота. Свойства, добыча, применение и цена серной кислоты
В городе Ревда с рельсов сошли 15 вагонов с серной кислотой. Груз принадлежал Среднеуральскому медеплавильному заводу.
ЧП произошло на ведомственных железнодорожных путях в 2013-ом году. Кислота разлилась на площади в 1000 квадратных километров.
Это указывает на масштабы потребности промышленников в реагенте. В Средние века, к примеру, в год требовались лишь десятки литров серной кислоты.
В 21-ом же веке мировая выработка вещества в год – десятки миллионов тонн. По объему производства и применения судят о развитии химических отраслей стран. Так что, реагент достоин внимания. Описание начнем со свойств вещества.
Свойства серной кислоты
Внешне 100-процентная серная кислота – маслянистая жидкость. Она бесцветна и тяжела, отличается крайней гигроскопичностью.
Это значит, что вещество поглощает из атмосферы пары воды. При этом, кислота выделяет тепло.
Поэтому, к концентрированной форме вещества воду добавляют малыми дозами. Влей много и быстро, полетят брызги кислоты.
Учитывая ее свойство разъедать материи, в том числе, и живые ткани, ситуация опасна.
Раствор серной кислоты до 40% — неконцентрированный, химически проявляет себя иначе. Воду в него доливать можно достаточно быстро.
Насыщенное же вещество взаимодействует и с неактивными. Исключение – благородные металлы. Почему же концентрат не «трогает» железо, медь?
Причина в их пассивации. Так называют процесс покрытия металлов защитной пленкой оксидов.
Она-то и препятствует растворению поверхностей, правда, лишь в обычных условиях. При нагреве реакция возможна.
Разбавленная серная кислота больше похожа на воду, нежели масло. Концентрат же, отличим не только по тягучести и плотности, но и дыму, исходящему от вещества на воздухе.
К сожалению, в Мертвом озере на Сицилии содержание кислоты меньше 40%. По внешнему виду водоема не скажешь, что он опасен.
Учитывая разъедающую способность водоема, местные преступники взялись сбрасывать в него трупы. Несколько дней, и от органики не остается и следа.
Качество горючего получаемого из обработанной органики низкое. Кислота в реакции является окислителем, хотя, может быть и восстановителем.
В последней роли вещество выступает, к примеру, взаимодействуя с галогенами. Это элементы 17-ой группы таблицы Менделеева.
Все эти вещества сами не являются сильными восстановителями. Если же кислота встречается с таковыми, выступает лишь в роли окислителя.
Пример: — реакция с сероводородом. А какие реакции дают саму серную кислоту, как ее добывают и производят?
Добыча серной кислоты
В прошлые века реагент добывали не только из железной руды, называемой пиритом, но и из железного купороса, а так же, квасцов.
В принципе, все перечисленные минералы являются серосодержащим сырьем, поэтому, могут применяться для производства серной кислоты и в современности.
Минеральная основа бывает разной, но итог ее обработки один – серный ангидрит с формулой SO2. Образуется при реакции серы с кислородом. Получается, нужно сжечь основу.
В обычных условиях сернистый ангидрид с ним взаимодействует медленно. Поэтому, промышленники окисляют сырье на катализаторах.
Однако, за последний метод «голосуют» лишь 20% промышленников. Основная же масса серной кислоты получается по контактной схеме.
Если подсчитать практику человечества по получению серной кислоты, «накапает» более 1000 лет.
Первые упоминания о реагенте и его добыче содержит труд, датируемый 940-ым годом.
Это записи одного из персидских алхимиков по имени Абубекер аль-Рази. Однако, о кислых газах, получаемых путем прокаливания квасцов, говорил и Джафар аль-Суфи.
Этот арабский алхимик жил еще в 8-ом веке. Однако, судя по записям, в чистом виде серную кислоту не получил.
Применение серной кислоты
Более 40% кислоты идут на производство минеральных удобрений. В ходу суперфосфат, сульфат аммония, аммофос.
Все это комплексные подкормки, на которые делают ставки фермеры и крупные производители.
В удобрения добавляют моногидрат. Это чистая, 100-процентная кислота. Кристаллизуется уже при 10 градусах Цельсия.
На производство всего одной тонны удобрения уходят 600 кило концентрата кислоты.
Около 30% серной кислоты тратятся на очистку углеводородов. Реагент улучшает качество смазочных масел, керосина, парафина.
К ним примыкают минеральные масла и жиры. Их тоже очищают с помощью серного концентрата.
Способность реагента растворять металлы применяется при переработке руд. Их разложение столь же бюджетно, как и сама кислота.
В главе «Свойства» указывалось, что при нагреве серная кислота справляется с оксидными пленками на латуни, меди, железе.
Поэтому, горячий реагент используют для их травления. Так именуют очистку металлических поверхностей. После обработки, сплавы и изделия из них выглядят как новые.
Способность кислоты поглощать воду из атмосферы, делает реагент отличным осушителем.
Если воздействовать на воздух 95-процентным раствором, остаточная влажность составит всего 0,003 миллиграмма паров воды на литр осушаемого газа. Метод применяют в лабораториях и на промышленных производствах.
Стоит отметить роль не только чистого вещества, но и его соединений. Они пригождаются, в основном, в медицине.
Бариевая каша, к примеру, задерживает рентгеновское излучение. Врачи заполняют веществом полые органы, облегчая исследования рентгенологов. Формула бариевой каши: — BaSO4.
Необходим минерал и строителям, использующим его в качестве связующего, скрепляющего материала, а так же, для декоративной отделки.
Цена серной кислоты
Цена на реагент – одна из причин его популярности. Килограмм технической серной кислоты можно приобрести всего за 7 рублей.
Столько за свою продукцию просят, к примеру, менеджеры одного из предприятий Ростова на Дону. Разливают канистрами по 37 кило.
Это стандартный объем тары. Встречаются, так же, канистры в 35 и 36 килограммов.
Купить серную кислоту специализированного плана, к примеру, аккумуляторную, немногим дороже.
За 36-килограммовую канистру просят, как правило, от 2000 рублей. Вот, кстати, еще одна сфера применения реагента.
Не секрет, что разбавленная дистиллированной водой кислота – это электролит. Он нужен не только для обычных батареек, но и машинных аккумуляторов.
Разряжаются они, поскольку серная кислота расходуется, при этом, выделяется более легкая вода. Падает плотность электролита, а значит, и его эффективность.
Применение в быту различных кислот
Наконец-то и до нас добрались морозы. По крайней мере, по сравнению с тем, что было до этого, кажется, что зима все-таки вспомнила про нас. После декабрьского дождя, слякоти и нуля градусов минус двадцать кажутся уже морозом.
А я вот болею. Как-то все разом навалилось – и физическая усталость, и психическая, расклеилась вся, куча болячек повылазила. Надо брать себя в руки и выбираться из этого. Говорят, кризис – прекрасный шанс изменить свою жизнь. Честно говоря, я в это не верю. Кто-нибудь сталкивался с этим? Что думаете по этому поводу? Поделитесь опытом.
А сегодня хочу предложить поговорить о кислотах. Некоторые могут сказать, что это – чисто химическая тема. А вот и нет. Кислоты в быту используются постоянно, мы сталкиваемся с ними практически каждый день. Но давайте начнем по порядку.
Что такое кислоты
Естественно, это химические соединения, в состав которых обязательно входит один или несколько атомов водорода, плюс так называемый кислотный остаток. В химических реакциях атомы водорода могут меняться на атомы металла, и получившиеся соединения буду называться солями.
Кислота – это не обязательно жидкость, в природе существуют и газообразные, и кристаллические их варианты. Например, я уже упоминала про фтор и фтороводородную кислоту, которую он образует. Вот если в этой кислоте поменять атом водорода на металл, например, тот же кальций или алюминий, то и получится фторид кальция, либо фторид алюминия, который и входит в состав зубной пасты.
С твердой кислотой вы можете познакомиться в статье про взаимодействие канцелярского клея с уксусом и даже провести с ней очень простые опыты.
Общее у них кислот одно – все они имеют более или менее кислый вкус, чем и объясняется их собирательное название. Схожи они между собой и своими химическими свойствами – практически все они разрушают металлы, а нашему организму приносят вред при попадании как на поверхность кожи или слизистых оболочек, так и вовнутрь.
Техника безопасности при работе с кислотами
Большинство кислот, особенно в виде концентрированных растворов, вызывают сильные ожоги, разрушают ткани организма. Потому так важно при работе с ними соблюдать меры безопасности.
Использование в быту
Чаще всего повседневной жизни можно столкнуться с использованием таких кислот:
Ну, особо продвинутые на здоровье граждане еще могут вспомнить никотиновую и фолиевую кислоту, а обладатели очумелых ручек – азотную и фосфорную. Если я что-то забыла – дополните в комментариях. Вполне возможно, я что-то упустила.
В природных соединениях можно найти такие кислоты как:
Расскажу о некоторых из них, наиболее интересных, на мой взгляд. Если хотите узнать о чем-то подробнее, напишите в комментариях, и я расскажу об этом.
Борная
Активно используется в медицине в качестве активного действующего вещества борной мази – известного антибактериального и антипаразитарного средства.
До недавних времен применялась и в виде 0,5%-ного спиртового раствора как антисептик. Сейчас практически не используется, так как последние исследования показали, что она приносит больше вреда, чем пользы. Если же вы все-таки решили ее использовать, то можете делать это только для наружного применения, но никак не внутреннего, чтобы не получить довольно сильное отравление.
Именно поэтому ее перестали использовать как консервант в губной помаде.
Используют ее и как удобрение, и как эффективный состав для борьбы с домовыми муравьями и тараканами.
Помню, когда-то еще лет двадцать назад, моя мама делала «шарики» из борной кислоты и раскладывала по кухне в надежде избавиться от внезапного нашествия муравьев.
Лимонная
Одна из более-менее безвредных для человека органических кислот. Она используется как подкисливающая пищевая добавка, например, в консервировании, в том числе и домашнем. Входит в состав многих моющих и чистящих средств.
Продается чаще всего в продуктовых магазинах в отделах с приправами. Представляет собой белые кристаллы.
Кстати, из нее и соды можно сделать классные бомбочки для ванны. Посмотрите об этом вот в этих статьях.
Активно применяется как народное средство для удаления пятен от ягод, вина, красок и чернил, ржавчины.
Про нее я в ближайшем времени планирую написать отдельную большую статью. Так что, если хотите поскорее узнать о ее выходе, подписывайтесь на обновления блога.
Муравьиная
Названа так потому, что впервые была получена из рыжих муравьев еще в далеком 17-м веке. Позже было установлено, что она содержится и в некоторых растениях. Например, всем знакомая крапива «обжигает» руки именно благодаря высокому содержанию муравьиной кислоты.
Так что, аллергикам и просто чувствительным людям нужно быть очень осторожными при «общении» с этой кислотой.
Где же вы можете с ней встретиться?
Например, в медицине. Она входит в состав некоторых медицинских препаратов, предназначенных для расширения сосудов, лечения невралгий и артритов, варикозного расширения вен, грибковых заболеваний, ушибов и отеков.
Предназначена она только для наружного применения.
Также применяется в качестве консервирующего и антибактериального препарата при заготовке кормов для сельскохозяйственных животных, в первую очередь – сена и силоса, которые после обработки этим составом менее подвержены быстрому гниению.
Используют ее и при окраске шерсти и в пчеловодстве для борьбы с паразитами. Для человека ядовита – вызывает серьезные раздражения кожи и ожоги (естественно, в зависимости от концентрации).
Уксусная
Присутствует на каждой кухне, либо в виде 70%-ной уксусной эссенции, либо как столовый уксус с концентрацией 6% или 9%, реже – 15-17 процентов.
Уксусные растворы широко применяется как приправа к блюдам, как чистящее средство (отлично удаляет с тканей фруктовые пятна), как средство для уменьшения жесткости воды, для профилактики образования накипи и ее удаления.
В старину меланхоличные барышни пили разбавленный уксус якобы для здоровья. На самом деле, никакой пользы здоровью это не приносит, а лишь раздражает слизистую желудка, что может привести к гастриту или язве.
Кстати, со свинцовой солью уксусной кислоты связана химическая загадка, которую часто задают начинающим химикам: «Какой сахар нельзя есть?».
У меня есть целый цикл статей об опытах с использованием уксуса, так что, если вам интересно, наберите в строке поиска на блоге, справа, в самом верху, «уксус» — и увидите много ссылок на интересные опыты, которые вы можете спокойно провести в домашних условиях самостоятельно.
Щавелевая
Идеальна для удаления с тканей пятен ржавчины и чернил. Хорошо растворяется в воде, что и используется в практических целях.
5%-ным раствором этой кислоты очищают трубы и сантехнику от ржавчины. Она входит в состав практически всех магазинных средств от ржавчины, почитайте ради интереса их состав. Так что, те, кто говорит: «Я не буду пользоваться всякой химией, а лучше возьму и почищу вещь просто щавелевой кислотой», не совсем правы.
Вы выигрываете только в цене, так как берете чистое вещество, без добавления ПАВ и отдушек, как в уже готовом чистящем средстве. К тому же, в стоимость магазинного средства входят затраты на рекламу, производство, транспортировку, упаковку и много-много всего остального.
А что касается «без химии» — то вам не повезло. И там, и там – абсолютно одинаковая химия.
Только нужно помнить, что это вещество очень ядовито, вызывает ожоги кожи и слизистых оболочек, а также пищевода, поэтому обращаться с ним нужно с осторожностью, работать в перчатках и желательно в респираторе, особенно с концентрированным веществом.
Да, чуть не забыла. В косметологии она тоже используется – для отбеливания кожи и удаления пигментных пятен. Естественно, в очень низкой концентрации.
Серная
Считается весьма опасной для человека: попадая на кожу, она вызывает серьезные ожоги, еще более вредна она для слизистых оболочек. Я даже писала о человеке, который ухитрился нечаянно выпить серную кислоту.
В быту она чаще всего используется для приготовления раствора электролита в автомобильные аккумуляторы:
Не знаю, как в других странах, а у нас концентрированная серная кислота считается прекурсором, поэтому купить ее просто так, без соответствующих документов, весьма проблематично, да и есть риск нарушить закон с неприятными для себя последствиями.
Так что, домашние опыты с концентрированной серной кислотой не могу предложить. Разве только посмотреть на видео. Вот довольно интересный опыт по обугливанию сахара.
Если говорить о промышленном применении серной кислоты, то ее недаром называют хлебом химической промышленности, так как без нее не обходится практически ни одно производство.
Ее используют для производства:
Без серной кислоты немыслима металлургия – с ее помощью извлекают металлы из руды. В нефтяной промышленности ее используют для очистки нефтепродуктов.
Кто-то еще сомневается, что химия нужна? Вы сможете прожить без пластмасс, тканей, лекарств? Только если переселитесь в лес и будете питаться ягодами и делать себе одежду их крапивных волокон, как в детской сказке. На такое способны лишь единицы людей.
Соляная
Весьма сильное соединение в плане химической активности. Ей не поддаются благородные металлы и медь, остальные растворяются ею без труда.
Концентрированная «солянка» смешивается с водой в любой пропорции для бытовых нужд. Сильный раствор этой неорганической кислоты без труда очищает фаянсовую сантехнику от известкового налета и ржавчины, а более слабым можно убрать с тканей пятна ржавчины, чернил, ягодного сока.
Если приглядитесь, на средстве для чистки унитазов «Туалетный утенок» написано, что в состав сходит соляная кислота, поэтому работать с ним нужно в резиновых перчатках и беречь глаза от попадания в них брызг.
Кроме того, без этой кислоты немыслима жизнь ни одного человека – она содержится в желудке и именно благодаря ей пища, попавшая в желудок, растворяется (переваривается).
К тому же, эта кислота служит первым барьером от болезнетворных бактерий, попавших в желудок – они погибают в кислой среде.
Ну а людям, страдающим от гастрита с повышенной кислотностью, эта кислота тоже хорошо знакома. Они даже уменьшают ее действие, чтобы она не разрушала стенки желудка, с помощью специальных препаратов, которые взаимодействуют с ней и уменьшают ее концентрацию.
Самые популярные – это препараты, содержащие оксиды магния и алюминия, например, «Маалокс». Впрочем, есть и экстремальщики, которые пьют пищевую соду, хотя уже доказано, что это приводит лишь к временному облегчению.
Азотная
Применяется в быту реже остальных, в первую очередь — для чистки ювелирных изделий и столового серебра. Также иногда используется для гравировки и хромировании металлических изделий.
Концентрированная азотная кислота вызывает сильные ожоги кожи. Кто работал с ней, знает, что, попадая на кожу, эта кислота оставляет на ней яркие желтые пятна.
Ну а в промышленности – эта кислота входит в тройку самых важных кислот наравне с серной и соляной. Ее используют для производства удобрений, взрывчатых веществ, травления и растворения металлов.
Вот вкратце рассказ о самых распространенных кислотах и их применении в быту. Я хотела показать, что химия не так далека от повседневной жизни, как многие думают, и кислоты – яркое подтверждение этому. Надеюсь, я достигла своей цели.
Если у вас есть что добавить – пишите в комментариях.
Всем хорошего настроения, не болейте!