Алюмосиликат

Получение алюмосиликата и его свойства
Алюмосиликат имеет вид мелкого порошка желтовато-белого оттенка, не имеющего запаха, нерастворимого в воде, но разлагающегося при взаимодействии с фтористоводородной кислотой.
Алюмосиликатами являются шпаты полевого типа (альбит, ортоклаз и т.д.), слюда и минералы глинистого типа.
Широкое применение алюмосиликаты получили в пищевой промышленности, где наиболее эффективно проявляются их свойства, направленные на препятствие к скатыванию и комкованию пищевых продуктов и ингредиентов. Также данное соединение обладает свойствами осветления и разделения сыпучих продуктов.
Алюмосиликат имеет характерный земляной привкус, не имеет примесей и может быть скомбинирован с другими видами силикатов.
Применение алюмосиликата
В пищевой промышленности алюмосиликат маркируется как пищевая добавка Е 559 и используется в сухих продуктах, порошках и смесях.
Применяют алюмосиликат при изготовлении сухих молочных продуктов (молоко, сливки и т.д.), а также сахарного песка, сахарной пудры, пищевой соли, пряностей и приправ. Этот силикат может входить в состав заменителя соли с подобными натуральному продукту свойствами.
Данный эмульгатор добавляют в состав сыров, а также в сырные полуфабрикаты, которые в нарезанном виде заворачивают в фольгу.
В соответствии с технологическими инструкциями и санитарно-эпидемиологическими нормами пищевая добавка Е 559 может входить в состав БАДов, сахарных таблеток, кондитерских изделий и консервированных продуктов.

В Европе применяют алюмосиликаты в медицинских и косметических целях. Их добавляют в мази и лечебные гели, белую глину, лекарственные препараты и крема. Алюмосиликат может содержаться в кормах и витаминных добавках для животных и птиц.
В качестве вспомогательного средства данные силикаты применяют при изготовлении упаковок, пакетов и бумажных изделий.
Противопоказания и ограничения в использовании
Алюмосиликаты необходимо употреблять в строго ограниченном количестве, так как они могут нанести серьезный вред здоровью человека. Использование в пищевой промышленности этой добавки разрешено во многих странах Европы, в том числе в Англии, России, Франции, Украине и т.д.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Кроме людей, от простатита страдает всего одно живое существо на планете Земля – собаки. Вот уж действительно наши самые верные друзья.
Первый вибратор изобрели в 19 веке. Работал он на паровом двигателе и предназначался для лечения женской истерии.
Человеческие кости крепче бетона в четыре раза.
Согласно исследованиям ВОЗ ежедневный получасовой разговор по мобильному телефону увеличивает вероятность развития опухоли мозга на 40%.
Вес человеческого мозга составляет около 2% от всей массы тела, однако потребляет он около 20% кислорода, поступающего в кровь. Этот факт делает человеческий мозг чрезвычайно восприимчивым к повреждениям, вызванным нехваткой кислорода.
Американские ученые провели опыты на мышах и пришли к выводу, что арбузный сок предотвращает развитие атеросклероза сосудов. Одна группа мышей пила обычную воду, а вторая – арбузный сок. В результате сосуды второй группы были свободны от холестериновых бляшек.
В стремлении вытащить больного, доктора часто перегибают палку. Так, например, некий Чарльз Йенсен в период с 1954 по 1994 гг. пережил более 900 операций по удалению новообразований.
По статистике, по понедельникам риск получения травм спины увеличивается на 25%, а риск сердечного приступа – на 33%. Будьте осторожны.
Печень – это самый тяжелый орган в нашем теле. Ее средний вес составляет 1,5 кг.
Ученые из Оксфордского университета провели ряд исследований, в ходе которых пришли к выводу, что вегетарианство может быть вредно для человеческого мозга, так как приводит к снижению его массы. Поэтому ученые рекомендуют не исключать полностью из своего рациона рыбу и мясо.
Самое редкое заболевание – болезнь Куру. Болеют ей только представители племени фор в Новой Гвинее. Больной умирает от смеха. Считается, что причиной возникновения болезни является поедание человеческого мозга.
На лекарства от аллергии только в США тратится более 500 млн долларов в год. Вы все еще верите в то, что способ окончательно победить аллергию будет найден?
Упав с осла, вы с большей вероятностью свернете себе шею, чем упав с лошади. Только не пытайтесь опровергнуть это утверждение.
Стоматологи появились относительно недавно. Еще в 19 веке вырывать больные зубы входило в обязанности обычного парикмахера.
Если улыбаться всего два раза в день – можно понизить кровяное давление и снизить риск возникновения инфарктов и инсультов.
АЛЮМОСИЛИКАТЫ
АЛЮМОСИЛИКАТЫ – природные и синтетические силикаты, содержащие в составе сложных анионов атомы алюминия и кремния.
Русский ученый Дмитрий Иванович Менделеев первым высказал идею, что алюмосиликаты представляют собой «неопределенные соединения», такие, например, как сплавы, но не простых тел, а близких по своим свойствам оксидов SiO2 и Al2O3. Сам термин «алюмосиликаты» был введен в минералогию Владимиром Ивановичем Вернадским, впервые правильно оценившим роль алюминия в построении минералов. В 1890-е он приступил к созданию своей теории строения алюмосиликатов. Как и Д.И.Менделеев, он говорил о близости химических функций оксидов кремния и алюминия. Отвергал мысль о том, что алюмосиликаты есть соли кремниевых кислот. По его мнению, алюмосиликаты являются производными сложных алюмосиликатных радикалов, «каолиновых ядер». Гипотеза о «каолиновом ядре» как о замкнутой группировке атомов кремния, алюминия и кислорода оказалась актуальной при расшифровке структуры полевых шпатов.
К началу 20 в. был накоплен обширный экспериментальный материал по составу и свойствам алюмосиликатов, однако их строение все еще оставалась загадкой. Решающее влияние на изучение структуры алюмосиликатов оказало открытие в 1912 немецкими физиками Максом фон Лауэ, Пaулем Книппингом (Knipping Paul) (1883–1935) и Вальтером Фридрихом (Friedrich Walter) (1883–1968) явления дифракции рентгеновских лучей на кристаллах и создание Уильямом Генри (Bragg William Henry) (1862–1942) и Уильямом Лоуренсом (Bragg William Lawrence) (1890–1971) Брэггами на этой основе принципиально нового метода исследования вещества – рентгеноструктурного анализа.
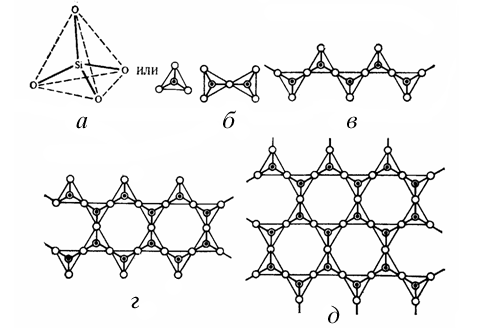
С 1925 по 1931 проводились интенсивные рентгеноструктурные исследования силикатов и алюмосиликатов и было установлено, что основным «строительным кирпичиком» этих соединений является атом кремния или алюминия, окруженный четырьмя атомами кислорода, – кремне(алюмо)кислородный тетраэдр SiO4(AlO4). Многообразие же алюмосиликатов объясняется разными способами соединения этих тетраэдров, которые обычно сочленяются вершинами с образованием связей Si-O-Si и Si-O-Al (рис. 1).
Алюмосиликаты распространены в природе, они составляют до 50% массы земной коры. К природным алюмосиликатам относятся, в первую очередь, полевые шпаты, имеющие каркасную структуру (например ортоклаз NaAlS3O8, альбит NaAlSi3O8, анортит CaAl2Si2O8).
У каркасных алюмосиликатов – непрерывный трехмерный каркас из тетраэдров, объединенных общими вершинами. Случаи связывания гранью или ребром неизвестны. Все атомы кислорода у тетраэдров кремния и алюминия являются общими. Так как в целом соединение должно быть электронейтральным, то полости между полиэдрами дополнительно заполняются катионами, которые нейтрализуют отрицательный заряд каркаса, возникающий при замене кремния на алюминий.
Каркасные алюмосиликаты являются основой многих поделочных камней. Такими алюмосиликатами являются и некоторые драгоценные камни, например берилл (Be3Al2)Si6O18 и его окрашенные разновидности: аквамарин (голубой, примесь оксида железа) и изумруд (зеленый, примесь оксида хрома). Полевые шпаты в составе различных горных пород, например, гранита, применяются в строительстве. Синтетические алюмосиликаты, полученные нагреванием оксидов алюминия и кремния с оксидами металлов, образуют основную кристаллическую фазу керамических материалов.
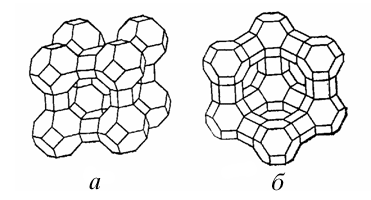
В 18 в. были открыты цеолиты – каркасные алюмосиликаты, состав которых можно описать общей формулой M I xM II y(Alx+2ySizO2x+4y+2z)·nH2O. Свое название они получили от греческих слов zeo – киплю и lithos – камень, т.к. образуют пузырчатое стекло при сильном и быстром нагревании. Известно более 40 минеральных видов природных цеолитов. Всего в мире известно около 1000 крупных месторождений цеолитов более чем в 40 странах, из них в России – около 20 (в Кузбассе, Якутии, Бурятии, Приморье, на Камчатке и о.Сахалин). С 1950-х в промышленных масштабах производятся искусственные цеолиты. В лабораториях синтезировано более 100 структурных видов, большинство которых не имеют природных аналогов.
Это позволяет им обменивать находящиеся в полостях решетки катионы металлов и молекулы воды. Натуральные и синтетические цеолиты широко применяются в качестве катионообменников, например, при умягчении воды.
Если из цеолитов полностью удалить адсорбированную в их полостях воду, они выступают в роли молекулярных сит: в освободившихся полостях могут селективно адсорбироваться молекулы диоксида углерода, аммиака и других веществ. Поэтому цеолиты применяются как адсорбенты в хроматографии, а также при очистке, осушке и разделении газов.
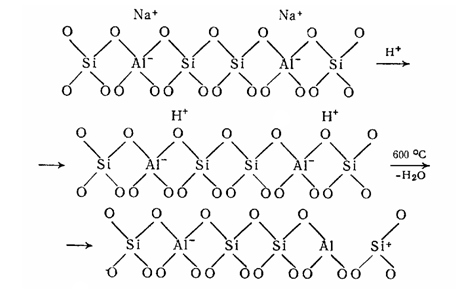
Цеолиты являются кислотными катализаторами. Подвижные катионы, например, катионы натрия при промывке цеолита растворами кислот обмениваются на катионы водорода с образованием кислот Бренстеда. Если такой цеолит нагреть, вода может покинуть кислотные центры Бренстеда, и останутся атомы алюминия, координированные только с тремя атомами кислорода (рис. 3).
Продукт реагирует как кислота Льюиса. Преимущество цеолитов по сравнению с другими катализаторами в том, что появившиеся каталитические центры многочисленны, равномерно распределены по каркасу и одинаковы по активности.
Многие цеолиты используются как носители катализаторов.
Разложение каркасных алюмосиликатов на поверхности Земли и их превращение в слоистые силикаты (глины и другие отложения) сопровождается огромными по масштабам эффектами связывания энергии. В связи с этим алюминию приписывается роль основного аккумулятора солнечной энергии в земной коре.
Горные породы любого типа: кристаллические, обломочные, глинистые и аморфные на поверхности литосферы разрушаются, поглощая солнечную энергию. Такой процесс часто называют выветриванием, хотя ветер участия в нем не принимает.
Обычно процесс начинается с физического дробления. При разрушении минералов вещество горных пород поглощает солнечную энергию, идущую на увеличение площади свободной поверхности.
Биохимическое разложение выражается в разрушении структуры минералов с образованием новых минералов (большей частью, глинистых), устойчивых в поверхностных условиях литосферы. В нем в той или иной степени принимают участие организмы как непосредственно, так и опосредствовано – через продукты своей жизнедеятельности (почвообразование (см.также ПОЧВЫ), свободный кислород, растворенные в водах органические кислоты и др.).
Например, кристаллический алюмосиликат альбит NaAlSi3O8 разрушается до аморфного опала – гидрооксида кремния SiO2·nH2O и глинистого минерала – каолинита состава Al2O3·2SiO2·2H2O. Переход кристаллических веществ в аморфные и тонкодисперсные сопровождается повышением энергонасыщенности вещества, т.к. расстояние между атомами в нем увеличивается. Происходит и геохимическая аккумуляция солнечной энергии, так как в полевых шпатах координационное число алюминия 4, а в образовавшихся за счет их глинистых минералах оно повышается до 6.
В слоистых алюмосиликатах кремне- и алюмокислородные тетраэдры соединены в одной плоскости в непрерывный слой. Слои тетраэдров обособлены друг от друга. Связь между слоями обеспечивается ван-дер-ваальсовыми силами или силами электростатического притяжения с помощью катионов, нейтрализующих отрицательные заряды слоев. Из-за наличия слоев тетраэдров и слабых связей между ними слоистые алюмосиликаты образуют чешуйчатые, листовые или таблитчатые агрегаты.
В увлажненном состоянии глины (состоящие из частиц размером менее 0,001 мм) пластичны. При высыхании они сохраняют приданную им форму, а при обжиге твердеют. Их используют для очистки различных продуктов (нефти, масел, вод и пр.), обезжиривания тканей, при производстве железорудных окатышей, керамзита, в литейном деле, медицине, изготовлении мыла, простого и огнеупорного кирпича, фаянса и других изделий.
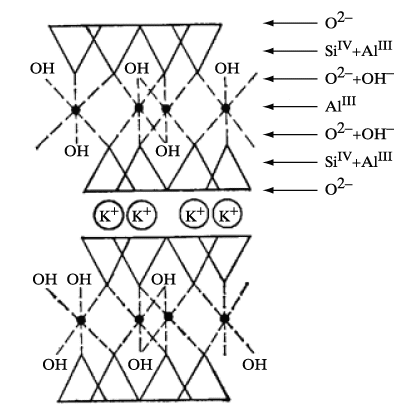
Минералы группы слюд образуют слоистую решетку с ионами «гостей» между силикатными листами «хозяина» (рис. 4).
Слюды легко расщепляются на очень тонкие, гибкие и в то же время упругие пластинки. Они обладают высокими диэлектрическими свойствами и огнестойкостью. В виде тонких пластин они прозрачны, поэтому было время, когда их использовали в качестве оконного стекла. Сейчас, благодаря высоким диэлектрическим свойствам, слюды применяются в электропромышленности, радиотехнике и приборостроении.
Зачем нужно жидкое стекло: секреты использования и область применения?
Современный рынок строительных материалов изобилует всевозможными смесями, содержащими сложные активные добавки. Однако среди всего этого есть материалы, которые остаются популярными веками например жидкое стекло – один из них. Его в строительстве применяют повсеместно, а иногда его и вовсе нечем заменить. Одно из достоинств – низкая себестоимость, что также является фактором выбора миллионов строителей по всему миру. Каждый, кто хочет стать профессионалом в строительстве, должен уметь им пользоваться.
Жидкое стекло: история возникновения и состав
Что такое жидкое стекло вы можете не знать, но пользовался им каждый. Хотя бы раз вам приходилось пользоваться силикатным клеем. Он продается в любом магазине канцелярских товаров. А ведь это и оно и есть. Удивительно то, что более двухсот лет тому назад люди разработали состав, который по сей день не менялся. А родиной изобретения является Германия. Там жил химик Ян Непомук фон Фукс, который занимался изучением силикатов и их свойств. Именно он смешал щелочной силикат с кремниевой кислотой.
В результате реакции наблюдалось схватывания смеси. Итог – формирование вязкой субстанции. Но если ее оставить на открытом воздухе, образуется твердое вещество, похожее на стекло, так как остается прозрачным. Однако производственный процесс выглядит сложнее, ведь составляющие приходится получать дополнительно. В чистом виде в природе они не встречаются. Требовалось разогреть кварцевый песок до полного расплавления. Применялись стеклоплавильные печи. Но после добавляли уголь и соду (сульфат натрия).
Состав жидкого стекла до сих пор неизменен. Однако печи стали усовершенствованные. Сейчас это автоклав, где точка кипения субстанции выше, что позволяет добиться лучших характеристик готового продукта. Но главное, что спустя два века эта технология до сих пор работает, и заменять ее другой, более дорогостоящей нет смысла. Жидкое стекло – это материал, используемый не только в строительстве. Есть масса производств, где требуется улучшить качество производимой продукции, и оно прекрасно дает это сделать практически без удорожания.
Характеристики жидкого стекла
Есть целый перечень достоинств данного материала. В список входит:
Среди сфер использования жидкого стекла применение в строительстве и промышленности определяется способностью заполнять нежелательные пустоты. Раковины, трещины, пазухи, заполненные силикатом, не увеличиваются со временем, не аккумулируют воду, и как следствие сохраняет морозостойкость монолита, если речь идет о бетонной поверхности.
Виды жидкого стекла
Принципиально состав может отличаться только вводимой добавкой, которую изготавливают на основе натрия, калия или лития. Соответственно различают и три различных типа продукции. Свойства жидкого стекла (калиевого K2O(SiO2)n, натриевого Na2O(SiO2)n, литиевого Li2O(SiO2)n) отличаются. Литий используется редко.
Основными являются два первых вида. Именно их можно встретить на прилавках строймаркетов. Именно они используются в строительстве и даже в быту. Поэтому необходимо рассмотреть данные типы более детально, и научиться распознавать, в каких случаях требуется то или иное соединение.
Жидкое натриевое стекло
При таком составе субстанция отличается повышенной вязкостью. Визуально он отличается неярко выраженным сероватым оттенком без видимых включений. Благодаря вяжущим свойствам одной из сфер применения является производство различных клеев, которые используют для организации гидроизоляционного покрытия. Как работать с жидким стеклом знает каждый профессиональный строитель. И, если нужно дополнительно защитить конструктив от влаги и воды, этот материал незаменим. Более того, железобетонная конструкция становится огнеупорной, и ее прочность повышается.
Жидкое калиевое стекло
Этот вид стал бы прекрасной альтернативой, если бы не более высокая стоимость производства. Смесь также тягучая, вязкая, клейкая. Только теперь она имеет едва заметный зеленоватый оттенок. Себестоимость повышается из-за сложности работы с калиевыми соединениями. С другой стороны этот состав обладает отличными бактерицидными свойствами. Материал не является благоприятной средой для поселения грибков, плесени, бактерий. Кроме того, благодаря химической нейтральности применение жидкого стекла в строительстве обусловлено необходимостью защитить сооружения от дождя, воздействию агрессивных сред, тумана, росы и т.д. Лакокрасочная продукция с этим компонентом отличается особым глянцем и блеском.
Область применения
Абсолютно естественно, что такой широкий спектр достоинства нашел применение в различных сферах деятельности человека. Сейчас обширное использование жидкое стекло нашло в таких областях:
Применение жидкого стекла в быту заключается не только в использовании силикатного клея для бумажных листов. Делая ремонт, каждый, кто желает придать конструкциям дополнительную прочность, влагозащитность, бактериальную безопасность, жаростойкость, обязательно покупает этот компонент.
Применения в строительстве
Если говорить о конкретных этапах возведения конструкций, применяется жидкое стекло для следующих видов работ:
Даже отмостка вокруг дома или дорожки на приусадебном участке прослужат на 8-10 лет дольше, так как раствор обретет гидрозащиту, что послужит причиной увеличения морозостойкости.
Когда для кладки используется жидкое стекло, способ применения заключается в том, что при условии сохранения правильных пропорций оно вводится в состав кладочного цементно-песчаного раствора. Тогда даже при сильном нагреве, как в случае с каминной кладкой, швы не растрескаются.
Если же требуется покрыть деревянные конструкции, его смешивают с окисью хрома, охрой или суриком. Такое покрытие не выцветает под действием влаги и не выгорает на солнце. Когда же требуется покрыть поверхность пленкой, делают водный раствор.
Применение в строительных смесях
Большой популярностью пользуются бетоны и растворы, в состав которых входит данный компонент. Цементно-песчаная смесь может использоваться для следующих видов общестроительных работ:
Также благодаря характеристикам жидкого стекла его успешно применяют при выкладке и облицовке дымоходов. Высоких температур оно не боится. Раствор не трескается, труба не сыпется, не трескается.
Как приготовить раствор с жидким стеклом
Решив использовать жидкое стекло как обязательный компонент строительной смеси, необходимо придерживаться технологии приготовления раствора. При этом главным фактором является его целевое назначение:
Чтобы субстанция была однородной, используйте строительный миксер или как минимум дрель со специальной насадкой для перемешивания. Руками это можно не успеть сделать, так как ввод жидкого стекла приводит к сокращению времени схватывания.
Применение в быту
При производстве сантехнических работ важно, чтобы все соединения были герметичны. Жидкое стекло – отличный герметик. Просто нанесите его на резьбу или фланец, соедините элементы, закрутите резьбу, удерживайте их в одном положении в течение нескольких минут. Так можно сделать герметичным водопровод и канализацию. Ограничение – газовые трубы. Здесь лучше пользоваться специализированными методами.
Также можно на силикат клеить, например, линолеум. Многие пользуются ПВА или Бустилатом, но они не в состоянии защитить от бактерий, грибка, плесени. В больших залах для торжеств, в театрах и других местах, где есть массивные шторы, текстиль обрабатывают стеклом, что не только защищает ткань от пыли, сохраняя привлекательный внешний вид. Силикат не горит, и в случае возгорания не даст шторам вспыхнуть.
В некоторых случаях лучше именно этим клеем соединять изделия из глины или керамики, деревянных брусков, кожи, резины, картона, фанеры, листов ДВП или ДСП. Даже посуду можно чистить стеклом (жидким, естественно). Для этого разведите его водой в пропорциях 25:1, опустите пригоревшую сковороду, кипятите 2 часа. Затем счистите отставший нагар обычной губкой. Если нужно очистить фарфор или стекло, время кипения уменьшают до 10 минут.
Преимущества и недостатки
К числу достоинств относится:
Однако есть и ряд недостатков:
Инструкция по обработке поверхностей жидким стеклом
Обрабатываемый объект необходимо подготовить. Счищается грязь и пыль. Если пришлось мыть, поверхности дают просохнуть. Разводят грунтовку, как сказано ранее и наносят состав кистью или валиком. Повторяют процедуру. Второй слой укладывается после полного высыхания первого. Приготавливают гидрозащитный раствор и нанося его на всю поверхность. Затем вымывают руки с мылом. До этого все нужно делать в перчатках.
Можно ли изготовить жидкое стекло самостоятельно
Более того, что это можно сделать, так еще и способ не один: